Một mẫu nước mưa có pH = 4,82. Môi trường của mẫu nước đó là:
A. trung tính.
B. bazơ.
C. axit.
D. không xác định được.
Một mẫu nước mưa có pH = 4,82. Môi trường của mẫu nước đó là:
A. trung tính
B. bazơ
C. axit.
D. không xác định được
Chọn đáp án C
pH = 4,82 < 7 ⇒ mẫu nước mưa có môi trường axit ⇒ Chọn C
Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H+ trong đó là:
A. 10-4M.
B. 10-5M.
C. > 10-5M.
D. < 10-5M.
pH = 4,82 → [H+] = 10-4,82M > 10-5M
Đáp án C
Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H + trong đó là
A. 10 - 4 M .
B. 10 - 5 M
C. > 10 - 5 M
D. < 10 - 5 M
Chọn C
pH = 4 , 82 → [ H + ] = 10 - 4 , 82 M > 10 - 5 M
Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H+ trong đó là:
A. 10-4M
B. 10-5M
C. > 10-5M
D. < 10-5M
Đáp án C
pH = 4,82 => [H+] = 10-4,82M > 10-5M
Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H + trong đó là :
A. [ H + ] = 1. 10 - 4 M.
B. [ H + ] = 1. 10 - 5 M.
C. [ H + ] > 1. 10 - 5 M.
D. [ H + ] < 1. 10 - 5 M.
Trộn 8g NaOH với 19,6g H2SO4, cho biết dung dịch thu được có môi trường: A. Axit B. Bazơ C. Trung hoà D. Không xác định được
\(n_{NaOH}=\dfrac{8}{40}=0,2mol\)
\(n_{H_2SO_4}=\dfrac{19,6}{98}=0,2\)\(mol\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,2 0,2
Dung dịch thu được là \(Na_2SO_4\) có môi trường trung hòa.
Cho HNO3 vào nước thu được dung dịch A. Môi trường của dung dịch A là
A. Trung tính
B. Axit
C. Muối
D. Bazơ
Một dung dịch có [OH- ]= 1,5.10-5. Môi trường của dung dịch này là:
A. Axit ; C. Kiềm
B. Trung tính ; D. Không xác định được
- Đáp án C
- Từ [OH-]= 1,5.10-5 (M) suy ra:
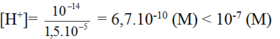
Vậy môi trường của dung dịch là kiềm.
Một dung dịch có [OH-] = 1,0.10 -5 M. Môi trường của dung dịch này là: A. Axit B. Không xác định được C. Trung tính D. Kiềm
Có [OH-] = 10-5
=> pH = 14 - 5 = 9 > 7
=> Môi trường dung dịch là kiềm
=>D